{{cell.content}}





撰文 | 一只鱼
#癌症#是造成世界人口死亡的主要原因之一,在癌症患者上常常会出现癌症细胞耐药性,使得很多治疗以失败告终,上皮间质转化(EMT)是上皮细胞失去上皮细胞特征并获得间充质细胞特征的过程,与癌细胞耐药性相关,但是EMT介导耐药性的机制仍不清楚。
2023年3月22日,来自比利时布鲁塞尔自由大学的Cédric Blanpain研究团队在Nature上发表题为RHOJ controls EMT-associated resistance to chemotherapy的文章,利用一个会自发性产生EMT的小鼠皮肤鳞状细胞癌模型,发现EMT肿瘤细胞对化疗具有高度耐药性,小GTP酶RHOJ调控EMT肿瘤细胞的耐药性,机制是因为RHOJ可以激活DNA损伤修复,促进复制胁迫反应。

为了研究体内EMT肿瘤细胞产生耐药性的机制,研究人员利用一种小鼠皮肤鳞状细胞癌(SCC)模型进行研究,该小鼠表达致癌的Kras变体(KrasG12D),并敲除抑癌基因Trp53,同时在毛囊谱系细胞中表达YFP。结合上皮细胞标记物EPCAM染色,YFP+EPCAM-细胞则为经历了EMT,失去了上皮细胞特征的肿瘤细胞。然后他们给该小鼠进行标准化疗药物处理,发现只有14%的SCC对化疗非常敏感,32%的SCC没有反应,并在化疗期间持续增殖,54%的SCC对化疗有部分反应。通过免疫染色和流失细胞分选(FACS)分析,他们发现对化疗有响应的是YFP+的上皮肿瘤细胞,而对化疗没有响应的是EMT肿瘤细胞,因此,EMT与SCC对化疗的反应相关。
接下来他们检测了EMT肿瘤细胞中化疗反应相关基因的表达情况,发现RHOJ(一种Cdc42亚家族的小GTP酶,介导黑色素瘤的化疗反应)在EMT肿瘤细胞中高表达,敲降Rhoj可以增强EMT肿瘤细胞的化疗反应,而过表达RHOJ可以降低肿瘤细胞对化疗的反应,并且Rhoj条件性敲除小鼠也表现出SCC对于化疗反应增强,因此,RHOJ介导EMT肿瘤细胞的化疗耐药性。
为了研究RHOJ促进EMT肿瘤细胞化疗耐药性的机制,他们进行了转录组和蛋白质组分析,发现在Rhoj敲降的EPCAM-细胞中转录水平下调的基因参与DNA复制、干扰素反应和肌动蛋白重塑,DNA复制相关蛋白水平也下调,并且Rhoj敲降导致差异表达的蛋白显著富集在复制压力下新复制的DNA相关蛋白中,说明RHOJ可能调控DNA复制和DNA修复。
接下来他们检测了DNA损伤标记物,磷酸化的组蛋白H2A.X(γ-H2AX),发现化疗之后与EPCAM+细胞相比,EPCAM-细胞的γ-H2AX显著降低,而敲除Rhoj之后,EPCAM-细胞的γ-H2AX水平又得到恢复,说明RHOJ阻止EMT肿瘤细胞中DNA损伤的累积。并且化疗之后,RHOJ还可以激活EMT肿瘤细胞中新一轮的DNA复制。
最后为了研究化疗后RHOJ如何调控DNA修复和激活DNA复制,他们检测了EMT肿瘤细胞中与RHOJ互作的蛋白,发现RHOJ与调控肌动蛋白纤维动态和核膜转运肌动蛋白的蛋白互作,而细胞核中的肌动蛋白可以调控DNA复制和修复,他们发现RHOJ调控细胞核内肌动蛋白的多聚化,抑制肌动蛋白多聚化可以使得EMT肿瘤细胞对化疗更敏感,且该过程依赖于RHOJ。
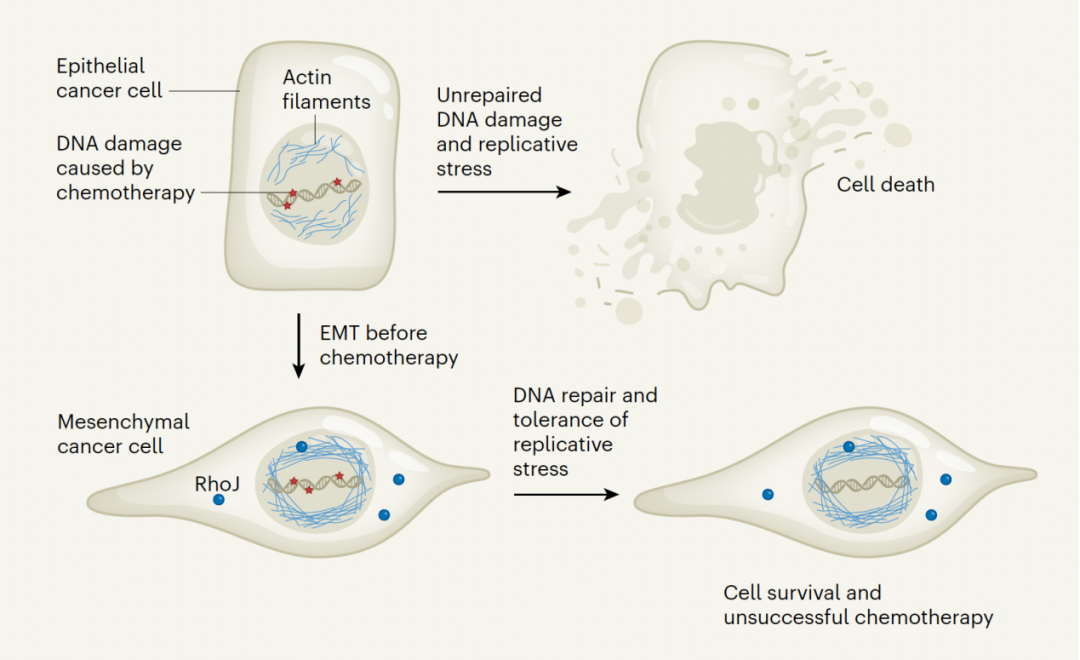
RHOJ调控肿瘤耐药性
总的来说,这项研究发现了EMT肿瘤细胞对化疗具有高度耐药性,RHOJ通过促进DNA损伤修复和复制介导了EMT肿瘤细胞的化疗耐药性,揭示了EMT肿瘤耐药性的新调控因子和背后的机制,为解决肿瘤耐药性问题提供新的思路和理论基础。
原文链接:
https://doi.org/10.1038/s41586-023-05838-7


想了解更多精彩内容,快来关注BioArt生物艺术
特别声明:本文为人民日报新媒体平台“人民号”作者上传并发布,仅代表作者观点。人民日报提供信息发布平台。

写下你的评论
{{cell.content}}
{{item.content}}
{{item.content}}